Guidelines & Standards
Evidence 2017;9(3): e1000164 doi: 10.4470/E1000164
Pubblicato: 28 marzo 2017
Copyright: © 2017 Lund et al. Questo è un articolo open-access, distribuito con licenza Creative Commons Attribution, che ne consente l’utilizzo, la distribuzione e la riproduzione su qualsiasi supporto esclusivamente per fini non commerciali, a condizione di riportare sempre autore e citazione originale.
Indipendentemente dal fatto che oggi i ricercatori – come Isaac Newton – si vedano “in piedi sulle spalle dei giganti”, quando pianificano un nuovo studio dovrebbero sempre tenere conto di tutte le conoscenze già disponibili. Benché il problema sia noto già dal 2005 (1,2), numerosi studi dimostrano che i ricercatori non utilizzano ancora metodi sistematici per identificare e fare riferimento a studi precedenti al fine di giustificare la reale necessità di un nuovo studio, o di interpretarne i risultati (3-11). Il problema riguarda anche studi clinici di elevata qualità pubblicati dalle riviste biomediche più prestigiose (4-12). Piuttosto, i ricercatori tendono a selezionare gli studi da citare sulla base di preferenze e considerazioni strategiche (13-18). Il termine evidence-based research (EBR) è stato coniato nel 2009 per indicare l’approccio che contrasta questa rilevante fonte di spreco nella ricerca biomedica (19), oltre che di rischi evitabili per i partecipanti.
Considerata la facilità di accesso ai database elettronici e alle revisioni sistematiche (RS) di elevata qualità — prodotte dalla Cochrane Collaboration e da numerosi centri internazionali di sintesi delle evidenze — non esiste più alcuna giustificazione per i ricercatori che non fanno riferimento a RS. Tuttavia, essi continuano imperterriti ad essere opportunistici (13,14), citando selettivamente gli studi che supportano l’intervento valutato (15-18). Alcuni finanziatori pubblici hanno già preso specifiche contromisure: ad esempio, i ricercatori che richiedono finanziamenti al National Institute for Health Research inglese devono giustificare la loro proposta con una RS delle evidenze disponibili, dimostrando di aver preso in considerazione le conoscenze già note (20). Tuttavia, la strada da fare è ancora molto lunga.
In questo contesto, un gruppo di ricercatori ha costituito l’EBR Network (www.ebrnetwork.org) per diffondere la consapevolezza e gestire questo problema che affligge la ricerca sanitaria. L’EBR Network ha l’obiettivo di ridurre gli sprechi nella ricerca promuovendo nuovi studi primari solo quando contemplino RS delle evidenze disponibili, oltre che una efficiente produzione, aggiornamento e diffusione delle RS stesse.
|
Key points
|
No a nuovi studi primari in assenza di una revisione sistematica delle evidenze disponibili
La metodologia delle RS prevede quesiti di ricerca predefiniti, criteri di inclusione, metodi di ricerca, procedure di selezione, valutazione di qualità, estrazione dei dati e analisi. In assenza di debita motivazione non devono essere esclusi gli studi pertinenti e i risultati di ogni studio che contribuiscono alle conclusioni della revisione (21,22). Di conseguenza, la formazione di base dei ricercatori deve prevedere la piena comprensione della necessità di una RS delle evidenze disponibili (21,23) e la capacità di valutare criticamente, interpretare e utilizzare le RS. Infatti, per ragioni scientifiche, etiche ed economiche le RS recenti di elevata qualità devono essere considerate indispensabili per giustificare la necessità di nuovi studi primari e per informare il loro disegno e l’interpretazione dei risultati (1-24).
La figura 1 mostra il processo della EBR dal quesito di ricerca preliminare sino alla decisione di procedere con un disegno di studio ottimale. La flow chart mira a supportare i ricercatori e non a contrastarli o pretendere di fornire tutte le risposte. La valutazione sistematica delle evidenze costituisce solo una delle variabili per definire un quesito di ricerca: infatti, i ricercatori possono utilizzare l’esperienza clinica, l’innovazione e le scoperte casuali, così come possono contare sui numerosi spunti che emergono dalle revisioni editoriali di un articolo.
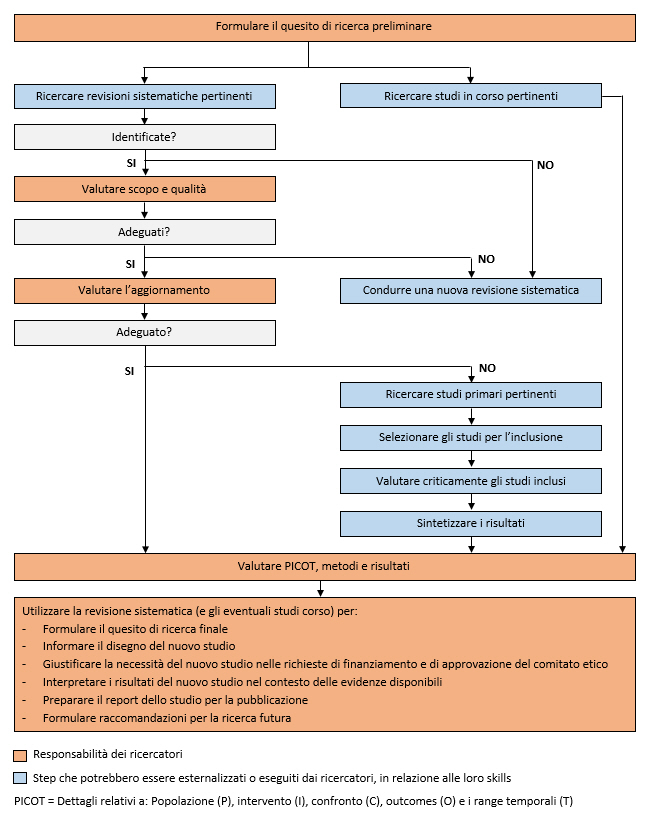
Considerato che il numero delle RS è aumentato vertiginosamente negli ultimi anni (26), nella maggior parte delle aree i ricercatori dovrebbero essere in grado di identificare almeno una RS pertinente. In ogni caso, anche quando le RS sono disponibili, i ricercatori possono incontrare varie difficoltà: ad esempio, le RS identificate possono essere obsolete o di qualità inadeguata, richiedendo così ulteriore impegno (che necessita di competenze rilevanti, tempo e risorse) prima di avviare lo studio primario. O ancora, la mancanza di indicatori comuni e di definizioni degli studi inclusi potrebbe precludere una sintesi statistica dei risultati, rendendo difficile integrare nuovi risultati. Prendere in considerazione anche gli studi in corso durante la produzione delle RS e quando si pianificano nuovi studi primari rappresenta un ulteriore sfida dell’EBR. In tal senso, se la registrazione dei nuovi trial clinici è ormai prassi consolidata (27), non è così per altre tipologie di studi.
Efficiente produzione, aggiornamento e diffusione delle revisioni sistematiche
La conduzione delle RS consuma risorse e tempo e molti ricercatori non sono adeguatamente formati. L’integrazione delle RS nel contesto della ricerca non sfida i ricercatori ad acquisire le competenze necessarie, ma è utile per garantire che ogni tentativo di accelerare i processi sottostanti non comprometta la qualità della ricerca. Questo richiede modifiche ai curricula formativi, stretta collaborazione tra ricercatori, bibliotecari, specialisti dell’informazione ed esperti informatici, oltre a una finalizzazione degli investimenti per ottimizzare e automatizzare alcuni processi durante la produzione delle RS.
Negli ultimi anni sono state messe in campo diverse iniziative, tra cui la serie di articoli per ridurre gli sprechi nella ricerca (28-34), che hanno portato al lancio della campagna REWARD (Reduce Waste and Reward Diligence, www.researchwaste.net). Altre organizzazioni (es. Cochrane Collaboration (35)) hanno l’obiettivo di condurre, aggiornare e diffondere con la massima efficienza le RS. Dalla consapevolezza che numerosi processi nella produzione di una RS potrebbero essere automatizzati è nata nel 2015 l’International Collaboration for the Automation of Systematic Reviews. Sono state sviluppate nuove modalità per la preparazione e l’aggiornamento delle RS, come le living systematic reviews (36,37). Le meta-analisi cumulative e altri metodi sono stati utilizzati per verificare la necessità di avviare nuovi studi38-41. Per i ricercatori che pianificano la conduzione di RS esistono software di facile utilizzo (www.systematicreviewtools.com). Infine, per evitare duplicazioni e assicurare che tutte le RS vengano pubblicate è possibile registrarle in PROSPERO (42) (www.crd.york.ac.uk/PROSPERO) e in SYRCLE (www.syrcle.nl), registro dedicato alle RS degli studi su animali.
Le responsabilità nell’evidence-based research
L’EBR Statement definisce le responsabilità di tutti gli stakeholder coinvolti nella ricerca (box). Il ricercatore è responsabile di pianificare e condurre una nuova ricerca solo se adeguatamente informata da tutti gli studi rilevanti sia precedenti sia in corso (figura 1). Ovviamente, non è necessario produrre una nuova RS se ne esistono già di adeguate. Tutti i ricercatori dovrebbero essere in grado di ricercare e valutare criticamente le RS, oltre che di interpretare i risultati del nuovo studio nel contesto di quelli della RS. La produzione e l’aggiornamento delle RS possono essere esternalizzati, anche se sarebbe auspicabile che tutti i ricercatori iniziassero la loro formazione producendo almeno una RS (23).
È fondamentale che non solo i ricercatori ma tutti gli stakeholder del processo scientifico – pazienti, finanziatori, agenzie regolatorie, comitati etici, editori – riconoscano le proprie responsabilità nell’EBR. Gli sprechi nella ricerca e i danni evitabili per i pazienti potrebbero essere prevenuti finanziando solo gli studi che includono una RS aggiornata. Esigere i riferimenti alle RS che sintetizzano tutti gli studi rilevanti deve diventare un principio guida per tutti coloro che salvaguardano il processo di ricerca, dalla formulazione del quesito sino alla pubblicazione.
Ricercatori senior e formatori devono garantire ai nuovi ricercatori un’adeguata preparazione a condurre evidence-based research (23). Gli specialisti dell’informazione e i bibliotecari hanno un ruolo chiave nell’insegnare agli studenti come effettuare una ricerca sistematica delle RS e nel condurre e pubblicare studi metodologici per migliorare le ricerche bibliografiche.
Last but not least, la ricerca e gli adeguati investimenti per automatizzare alcuni processi di conduzione delle RS sono rilevanti per raggiugere e mantenere l’EBR, in quanto il volume crescente della letteratura e l’aumentata complessità degli interventi in studio (26) rendono impossibile gestire il carico di lavoro utilizzando i tradizionali metodi manuali di revisione.
|
EVIDENCE-BASED RESEARCH STATEMENT Avviare uno studio in assenza di RS che mostrano l’esistenza di una reale incertezza, in particolare quando la ricerca coinvolge persone o animali, è non etico e non scientifico e genera sprechi. Ricercatori, finanziatori, enti regolatori, comitati etici, editori, istituzioni di ricerca, formatori e specialisti dell’informazione spesso non utilizzano in maniera sistematica la ricerca precedente quando avviano, finanziano o pubblicano i risultati di nuovi studi. Di seguito definiamo le responsabilità degli stakeholder per raggiungere i due obiettivi dell’EBR: 1. Nessun nuovo studio primario è giustificato in assenza di un’adeguata RS delle evidenze esistenti che ne dimostri la reale necessità. 2. Efficiente produzione, aggiornamento e diffusione delle RS. OBIETTIVO 1: Nessun nuovo studio primario è giustificato in assenza di un’adeguata revisione sistematica delle evidenze esistenti che ne dimostri la reale necessità Ricercatori
Finanziatori della ricerca
Autorità regolatorie e comitati etici
Editori e revisori
Formatori
Pazienti
OBIETTIVO 2: Efficiente conduzione, aggiornamento e diffusione delle revisioni sistematiche Specialisti delle revisioni sistematiche
Bibliotecari e specialisti dell’informazione
Tecnici informatici, programmatori e ingegneri informatici
Finanziatori
RACCOMANDAZIONI
|
Invito all’azione
Il compito di identificare e rispondere alle sfide di tutti gli stakeholder può essere affrontato in maniera efficace solo attraverso una collaborazione internazionale. L’EBR Network ha tracciato una roadmap per le pubblicazioni (tra cui una RS dello stato dell’arte e dell’impatto della stessa EBR) al fine di aumentare la consapevolezza delle sfide per i diversi stakeholder (implication papers) e per suggerire come gestire le attività previste dall’EBR statement (how-to papers). Per ulteriori dettagli: www.ebrnetwork.org.
Contributo degli Autori
Questo statement è stato elaborato in occasione del meeting inaugurale di Bergen (dicembre 2014), organizzato da MWN, GJ e HL. Tutti gli autori hanno partecipato al meeting e allo sviluppo dell’EBR statement.
Disclosure dei conflitti di interesse
Gli autori hanno letto e compreso la policy del BMJ sulla dichiarazione dei conflitti di interesse e non hanno conflitti da dichiarare. L’EBR network non accetta finanziamenti dall’industria farmaceutica e biomedicale.
Indirizzo per la corrispondenza
hlund@health.sdu.dkProvenienza
Tradotto con permesso da Lund H, Brunnhuber K, Juhl C et al. Towards evidence based research. BMJ 2016;355:i5440.Fonti di finanziamento
Research Council of Norway, Bergen University College, Norwegian Knowledge Centre for the Health Services, Musculoskeletal Statistics Unit, Parker Institute (sostenuto dalla Oak Foundation) gruppo di ricerca SEARCH (Synthesis of Evidence and Research) della University of Southern Denmark.Approvazione comitato etico
-Ringraziamenti
Ringraziamo i partecipanti del meeting di Bergen e i membri dell’EBRNetwork per il loro aiuto nella creazione di questo documento. Ringraziamo inoltre per il supporto finanziario il Research Council of Norway, il Bergen University College, il Norwegian Knowledge Centre for the Health Services, la Musculoskeletal Statistics Unit, il Parker Institute (sostenuto dalla Oak Foundation) e il gruppo di ricerca SEARCH (Synthesis of Evidence and Research) della University of Southern Denmark, per aver reso possibile la creazione di questo statement e dell’EBRNetwork.
Note alla versione italiana
La Fondazione GIMBE ha realizzato la traduzione italiana dell’EBR Statement senza alcun finanziamento istituzionale o commerciale.
Team che ha realizzato la versione italiana
Responsabile scientifico
Antonino Cartabellotta, Fondazione GIMBE
Coordinamento editoriale
Marco Mosti, Fondazione GIMBE
Traduzione
Corrado Iacono, Comitato Etico Bologna-Imola
Revisione editoriale
Elena Cottafava, Fondazione GIMBE
Pagina aggiornata il 28/marzo/2017



